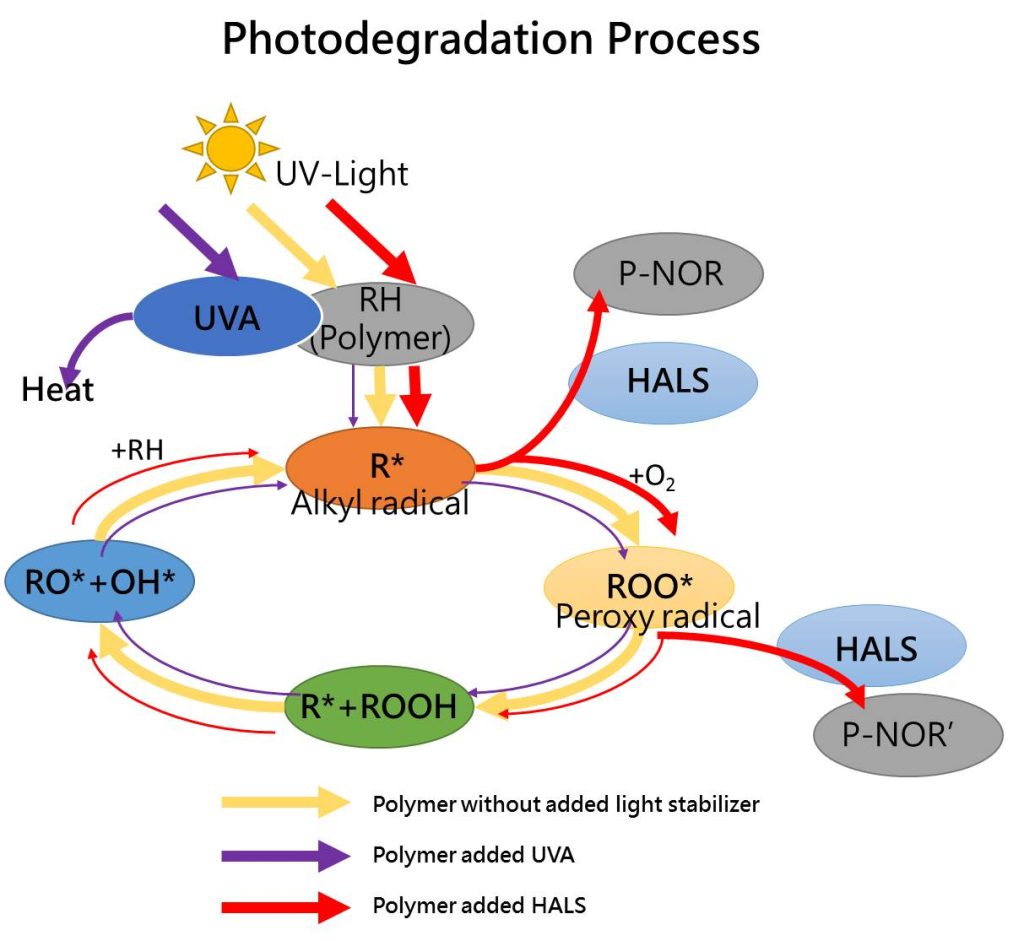
بهطور کلی گرما، نور، هوا و آب مهمترین عوامل در تخریب پلیمرها هستند. تقریباً تمام پلیمرهای مصنوعی در برابر اثرات نامطلوب محیط مانند گرما، نور، اکسیژن و… نیاز به موادی بهعنوان تثبیتکننده دارند. این تثبیتکنندهها افزودنیهای شیمیایی هستند که به مواد پلیمری مانند پلاستیکها اضافه میشوند تا تخریب آنها را مهار یا به تأخیر اندازند.
تثبیتکنندهها
تثبیتکنندهها در تمام مراحل چرخه پلیمر استفاده میشوند. این ترکیبات منجر به تولید سریعتر و با نقص کمتر تولید، افزایش طول عمر مفید پلیمرها و تسهیل در بازیافت آنها میشوند. انواع مختلفی از پلاستیک وجود دارد و هر کدام ممکن است در برابر چندین نوع تخریب آسیب پذیر باشند، که معمولاً منجر به استفاده از چندین تثبیتکننده مختلف در ترکیب میشود. حتی برای محصولاتی که از یک نوع پلاستیک ساخته شدهاند، کاربردهای مختلف ممکن است نیازهای تثبیت متفاوتی داشته باشند. بهعنوان مثال، در مورد محصولات پلیاولفینی برای استفاده در فضای باز، یک آنتی اکسیدانت فنولیک (جذبکننده رادیکال) و آنتی اکسیدانت فسفر (تجزیهکننده پراکسید) با هم مخلوط میشوند تا بهعنوان تثبیتکنندههای حرارتی در طی فرآیندهایی مانند قالبگیری عمل کنند و یک جاذب ماوراء بنفش و HALS نیز برای ارائه بهبود شرایط جوی در حین استفاده مخلوط میشوند [1].
دستهبندی تثبیتکنندهها
بهمنظور انتخاب مؤثرترین تثبیتکننده، مهم است که بدانیم پلیمر در معرض چه محدوده دمایی قرار خواهد گرفت. یک تثبیتکننده خوب باید پلاستیک را در حین پردازش، جایی که دمای بالا برای ذوب شدن و تشکیل رزین وجود دارد و در طول عمر زمانی که در معرض دمای بالای سرویس قرار میگیرد، محافظت کند.
امروزه دستهبندیهای متفاوتی برای تثبیتکنندهها تعیین شده است. اگر بخواهیم تثبیتکنندهها را براساس عملکرد دستهبندی کنیم، شامل تثبیتکنندههای نوری، آنتی اکسیدانتها، آنتی ازونها، جاذبهای رادیکال، حذفکنندههای پراکسید، جاذبهای اسید و بازدارندههای آتش میشوند. در ادامه به معرفی این تتثبیتکنندهها پرداخته خواهد شد.
آنتی اکسیدانت
آنتی اکسیدانتها مانع از خوداکسایشی پلیمر در واکنش با اکسیژن اتمسفر میشوند. تخریب هوازی بهتدریج در دمای اتاق اتفاق میافتد، اما تقریباً تمام پلیمرها هنگام پردازش در دمای بالا در معرض خطر اکسیداسیون حرارتی قرار دارند. در قالبگیری یا ریختهگری پلاستیکها (بهعنوان مثال قالبگیری تزریقی) نیاز است که پلاستیک بالاتر از نقطه ذوب (حدود 200 تا 300 درجه سانتیگراد) باشند. در این شرایط واکنش با اکسیژن بسیار سریعتر اتفاق میافتد. حتی با اینکه تلاش میشود سطح اکسیژن کاهش یابد، حذف کامل آن غالباً غیرقابل دستیابی است و حتی غلظت بسیار کم اکسیژن نیز میتواند برای شروع تخریب کافی باشد. حساسیت به اکسیداسیون، بسته به نوع پلیمر مورد نظر، بهمیزان قابل توجهی متفاوت است. بدون تثبیتکنندهها، پلیپروپیلن، پلیاتیلن و پلیمرهای غیر اشباع مانند لاستیک طبیعی در دمای اتاق بهآرامی تخریب میشوند، در صورتی که پلیاستایرن حتی در دمای بالا نیز میتواند پایدار باشد. بهویژه در پلیپروپیلن، بهدلیل واکنش سریع رادیکال آلکیل با اکسیژن، از بین بردن رادیکال آلکیل اولیه (R•) دشوار است و تنها با استفاده از آنتی اکسیدانتهای تخصصی این مهم بهدست میآید.
این آنتی اکسیدانتها به دو دسته آنتی اکسیدانت اولیه (بازدارندههای رادیکال ) و آنتی اکسیدانت ثانویه (حذفکننده هیدروپراکسیدها) تقسیم میشوند [3].
آنتی اکسیدانت اولیه (حذفکننده رادیکال)
آنتی اکسیدانتهای اولیه بهعنوان جاذب رادیکالها عمل میکنند و رادیکالهای پراکسی (ROO•) و همچنین رادیکالهای آلکوکسی (RO•)، رادیکالهای هیدروکسیل (HO•) و رادیکالهای آلکیل (R•) را حذف میکنند. آنتی اکسیدانتهای اولیه تجاری شامل ترکیبات فنولی و آمینهای آروماتیک ثانویه هستند. این ترکیبات دارای طیف وسیعی از وزن مولکولی، ساختار و عملکرد هستند. موثرترین آنتی اکسیدانتهای اولیه آمینهای آروماتیک ثانویه هستند. با این حال، آنها باعث تغییر رنگ قابل توجهی میشوند و فقط در صورتی میتوان از آنها استفاده کرد که تغییر رنگ مشکلی نداشته باشد، مانند محصولات لاستیکی پر از دوده و کربن. آنها همچنین بهعنوان آنتی ازون و غیرفعالکننده یونهای فلزی نیز عمل میکنند. این آنتی اکسیدانتها هیدروژن را به رادیکالهای آلکوکسی و هیدروکسی اهدا میکنند و در نتیجه آنها را بهترتیب به الکلهای بی اثر و آب تبدیل میکنند. در شکل 1، مکانیسم حذف رادیکالهای پراکسی توسط یک آنتی اکسیدانت اولیه نشان داده شده است [3].
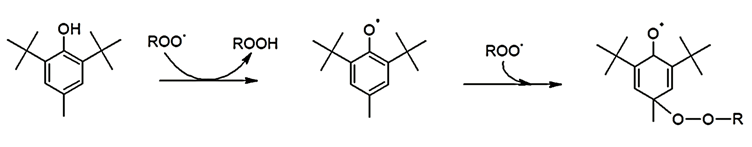 شکل 1. عملکرد یک نوع آنتی اکسیدانت اولیه [4].
شکل 1. عملکرد یک نوع آنتی اکسیدانت اولیه [4].
آنتی اکسیدانت ثانویه (حذفکننده هیدروپراکسیدها)
این آنتی اکسیدانتهای ثانویه، هیدروپراکسیدها (ROOH) را قبل از تجزیه به رادیکالهای آلکوکسی و هیدروکسیل، به محصولات غیر واکنشی تجزیه میکنند. آنها اغلب در ترکیب با حذفکنندههای رادیکال آزاد (آنتی اکسیدانتهای اولیه) برای دستیابی به یک اثر همافزایی استفاده میشوند. رایجترین آنتی اکسیدانتهای ثانویه ترکیبات فسفر نوع سوم (فسفیتها) هستند. آنها هیدروپراکسیدها را به الکلهای مربوطه کاهش میدهند و خود به فسفات تبدیل میشوند.
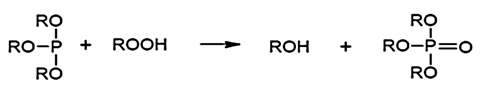 شکل 2. مکانیسم کلی تجزیه پراکسید [4].
شکل 2. مکانیسم کلی تجزیه پراکسید [4].
دسته دیگری از آنتی اکسیدانتهای ثانویه تیواترها یا سولفیدهای آلی (RSR) هستند. آنها دو مولکول هیدروپراکسید را به الکلهای مربوطه تجزیه میکنند و به سولفوکسیدها و سولفونها تبدیل میشوند [3].
 شکل 3. مکانیسم تجزیه هیدروپراکسیدها به الکلهای مربوطه توسط آنتی اکسیدانت ثانویه [4]
شکل 3. مکانیسم تجزیه هیدروپراکسیدها به الکلهای مربوطه توسط آنتی اکسیدانت ثانویه [4]
ضد ازونها (antiozonant)
ازون و نور خورشید بهسرعت به پلیمرهای محافظت نشده حمله میکنند که میتواند عمر مفید آنها را به میزان قابل توجهی کاهش دهد. بهویژه پلیمرهای با ظرفیت غیراشباع بالا، یعنی لاستیکها، مستعد تخریب ازون هستند، زیرا پیوندهای دوگانه در پلیمرهای غیراشباع بهراحتی با ازون واکنش میدهند. برای جلوگیری یا کاهش سرعت تخریب اکسیداسیون ناشی از ازون، آنتی ازونها اغلب اضافه میشوند.
آنتی ازون یک ترکیب آلی است که از آسیبهای ناشی از ازون جلوگیری میکند یا آن را به تأخیر میاندازد. مهمترین آنتی ازونها آنهایی هستند که از تخریب الاستومرها مانند لاستیک جلوگیری میکنند. بهویژه آنتی اوزونها در تولید تایر استفاده میشوند. قویترین و رایجترین دسته آنتی ازونها پارا فنیلن دیآمینها (PPDs) هستند که ساختار کلی زیر را دارند.
 شکل 4. ساختار ضد ازون [5]
شکل 4. ساختار ضد ازون [5]
پارافنیل دیآمینها نه تنها آنتی ازونهای کارآمد هستند، بلکه آنتی اکسیدانتهای اولیه بسیار مؤثری نیز هستند. فعالیت انواع مختلف PPD به حلالیت آنها در لاستیک، دما و شرایط پیری نیز بستگی دارد.
حداقل سه مکانیسم رقابتی برای محافظت از ازون وجود دارد:
1- آنتی ازونها سریعتر از لاستیک با ازون واکنش نشان میدهند و بنابراین بهعنوان جاذب ازون عمل میکنند.
2- محصولات واکنش آنتی ازونها یک لایه محافظ روی لاستیک تشکیل میدهند که از واکنش ازون با لاستیک جلوگیری میکند.
3- آنتی ازونها با محلهای رادیکال قطعات لاستیک واکنش میدهند و پیوندهای متقابل جدیدی را تشکیل میدهند و در نتیجه شبکه لاستیکی را بازسازی میکنند.
واکنش بین پارا فنیلن دیآمینهای جایگزین آلکیل با نیتروژن و ازون در زیر نشان داده شده است:
ازون گروه آمین فنیلن دیآمین را اکسید کرده و هیدروکسیل آمین تولید میکند. حذف بعدی آب باعث تولید کینو دیایمین میشود که میتواند توسط رادیکالهای پراکسیل بیشتر اکسید شود و نیترونها و دینیترونها را تولید کند (نمایش داده نشده است) [5].
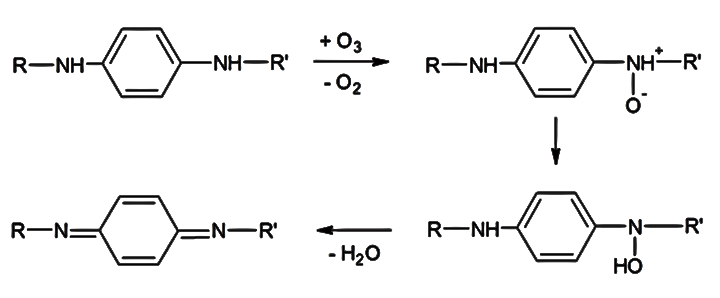 شکل 5. مکانیسم واکنش پارا فنیل دیآمینها [5].
شکل 5. مکانیسم واکنش پارا فنیل دیآمینها [5].
سردکنندههای ناگهانی (Quencher)
سردکنندهها، مولکولهایی هستند که انرژی را از کروموفور حالت برانگیخته شده میپذیرند. کروموفور بعد از انتقال انرژیاش به حالت پایه خود یعنی حالت انرژی پایدار بر میگردد. Quencherها انرژی را به گرما، فلورسانس یا فسفرسانس تبدیل و آزاد میکنند، و با این روش از تخریب پلیمر جلوگیری میکنند [6].
تثبیتکننده پرتو فرابنفش
تثبیتکنندههای فرابنفش موادی هستند که میتوانند نور آسیبزننده به پلیمر را جذب یا خنثی کنند. اگر چه برخی از پوششها از طریق رنگ کردن یا روکش با فلزات روی سطح و یا وجود یک رنگدانه با خاصیت بازتاب بالای پرتو UV نیز کاربردی هستند [6]. در ادامه انواع تثبیتکنندههای نوری شرح داده میشوند.
ترکیبات HALS
در واقع این کلمه مختصر شده Hindered amine light stabilizers است. هالسها بازدارندههای بسیار مؤثری در برابر تخریب پلیمرها در دماهای پایین و متوسط ناشی از رادیکالهای آزاد هستند. این دسته از تثبیتکنندههای آمینی بر اساس مشتقات 2،2،6،6 تترمتیل پیپریدین میباشند. آنها اغلب بهعنوان تثبیتکننده نور، بهویژه برای پلیاولفینها استفاده میشوند. این تثبیتکنندهها ترکیبات شیمیایی شامل یک گروه عاملی آمین هستند. برخلاف سایر تثبیتکنندهها پرتو فرابنفش را جذب نمیکنند، بلکه با حذف مداوم و چرخهای رادیکالهای آزاد ایجاد شده در اثر اکسیداسیون، از تخریب پلیمرها جلوگیری میکنند [6].
دستهبندی هالسها:
هالسها را میتوان بر حسب وزن مولکولیشان دستهبندی کرد:
- هالسها با وزن مولکولی کم حدود 200-500 گرم بر مول (MW HALS Low)
- هالسها با وزن مولکولی برابر یا بزرگتر از 2000 گرم بر مول (High MW HALS)
این دو نوع دارای سرعت انتشار متفاوتی در ماتریس پلیمری هستند که عامل مهمی در محافظت از پلیمرها در برابر پرتو UV است. در کل هالسها با وزن مولکولی بالا بهعنوان تثبیتکننده حرارتی طولانی مدت، نسبت به هالس با وزن مولکولی پایین مؤثرتر است؛ در حالی که هالس با وزن مولکولی بسیار پایین، به هیچ وجه پایداری حرارتی زیادی را ایجاد نمیکند. کارایی هالسها همچنین میتواند به شدت تحت تأثیر ساختار، یعنی گروههای جانبی و گاهی اوقات تحت تأثیر فرمولاسیون و شرایط سطح قرار گیرد. برای به حداکثر رساندن پایداری نوری پلاستیکها، باید مناسبترین ساختار هالس انتخاب شود.
فوتواکسیداسیون معمولاً از سطح با ترکهای قابل مشاهده شروع میشود که منجر به تخریب سریع خواص مکانیکی خواهد شد. در تئوری، پلیاولفینهایی مانند پلیاتیلن (PE) و پلیپروپیلن (PP) هنگام قرار گرفتن در معرض نور خورشید تا حد قابل قبولی پایدار هستند، زیرا هر دو پیوند C-C و C-H تابش UV خورشید را در همه طول موجها جذب نمیکنند. با این حال همیشه آلودگیهایی مانند کاتالیزور باقیمانده، رنگدانهها و تخریب حرارتی توسط محصولات حاصل از فرآوری مذاب رزینها وجود دارد که میتواند باعث تخریب نوری هر پلیالفین در مواجهه با نور فرابنفش شود که بهنوبه خود باعث بریدگی زنجیره و یا اتصال عرضی شود و در نهایت ترکهای سطحی و از دست دادن خواص مکانیکی را ایجاد کند [7].
راندمان بالای هالسها مبتنی بر مجموعه پیچیدهای از واکنشهای مهار رادیکالهای آزاد است که با اکسیداسیون هالسها به رادیکالهای نیتراکسید (RNO·) که در اثر واکنش با پراکسیدها یا هیدروپراکسیدها شروع میشود (شکل پایین). این ترکیبات متعاقباً با رادیکالهای آلکیل پلیمری واکنش داده و اترهای هیدروکسیآمین تولید میکنند که میتوانند با انواع ترکیبات واکنش دهند. رادیکالهای RNO· جدید ممکن است از واکنش اترهای هیدروکسیآمین با رادیکالهای آلکیلپروکسی و آسیلپروکسی (چرخه دنیسوف) بازسازی شوند.
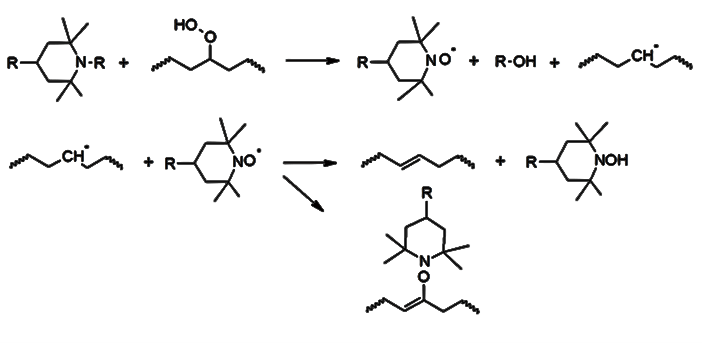 شکل 6. اکسیداسیون هالسها و تولید اترهای هیدروکسی امین [7].
شکل 6. اکسیداسیون هالسها و تولید اترهای هیدروکسی امین [7].
اکسیداسیون هالسها به رادیکالها یک واکنش نسبتاً کند و وابسته به دما است. علاوه بر این، آنها در دماهای بالا (بالاتر از 80 درجه سانتیگراد یا بیشتر) بسیار کارآمد نیستند. به همین دلیل، HALS اغلب در ترکیب با آنتی اکسیدانهای اولیه و ثانویه استفاده میشود.
 شکل 7. چرخه اکسیداسیون هالسها [7].
شکل 7. چرخه اکسیداسیون هالسها [7].
جاذبهای نور UV
تثبیتکنندههای ماوراء بنفش بهطور معمول با انتقال پروتون درون مولکولی برگشتپذیر، انرژی پرتو فرابنفش را بهعنوان گرما جذب و پراکنده میکنند. این جاذبها باید نور را در محدوده 290-400 نانومتر جذب کنند و نسبت به سایر تشعشعات شفاف باشند. از این جاذبهای رایج میتوان به بنزوفنونها و بنزوتریازولها اشاره کرد. در شکل 8 انواع جاذبهای نور UV مشاهده میشود.
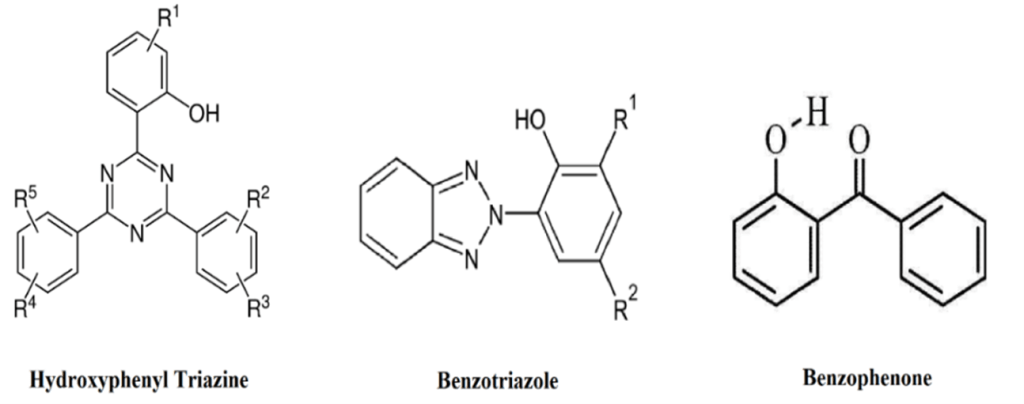 شکل 8. ساختار انواع جاذبهای فرابنفش [8].
شکل 8. ساختار انواع جاذبهای فرابنفش [8].
همانطور که در شکل زیر مشاهده میشود جاذبهای UV بهصورت پوششی روی محصول پلیمری قرار میگیرند و پرتوهای فرابنفش جذب شده را بهصورت گرما و انرژی ضعیف شده آزاد میکنند [8].
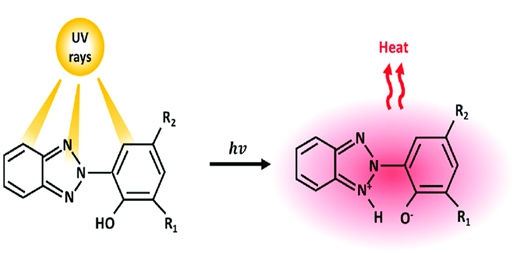 شکل 9. عملکرد جاذب پرتو فرابنفش [9].
شکل 9. عملکرد جاذب پرتو فرابنفش [9].
در شکل 10 چرخه پایدارسازی پلیمر توسط تثبیتکنندههای نوری مشاهده میشود. اگر جهت فلشهای زرد رنگ را مشاهده کنید، چرخه تخریب پلیمر توسط نور را میبینید. در ادامه اگر جهت فلش بنفش رنگ را دنبال کنید، چرخهای را مشاهده میکنید که به پلیمر جاذب فرابنفش اضافه شده است و فلش قرمز رنگ هم نشاندهنده اضافه کردن تثبیتکنندههای آمینی (HALS) به پلیمر است که این تثبیتکننده چرخه تخریب نوری را در مرحله دوم در اثر ترکیب شدن با رادیکال آزاد قطع میکند.
در واقع هالسها در اثر ترکیب شدن با رادیکال پراکسی ROO. و رادیکال آلکیل R. و تولید رادیکالهای آمینوکسیلهای مربوطه از ادامه یافتن چرخه تخریب نوری جلوگیری میکنند. رادیکالهای آمینوکسیل تولید شده میتوانند از طریق یک سری واکنشهای رادیکال اضافی دوباره به فرم آمین خود برگردند و این همان خاصیت طول عمر بالای هالسها است.
پلیمرها در مسیرهای مختلفی فراتر از اکسیژن و نور مستعد تخریب هستند. بنابراین از تثبیتکنندههای متفاوتی برای افزایش طول عمر پلیمرها استفاده میشود.
رباینده اسید (acid scavengers)
در واقع این آنتی اسیدها ناخالصیهای اسیدی را خنثی میکنند، مخصوصاً آنهایی که HCl آزاد میکنند. آنتی اسیدهای متداول عبارتند از صابونهای فلزی (نمک فلزی یک اسید چرب) مانند استئارات كلسيم و استئارات روی، عوامل معدنی مانند هيدروتالکیت و هيدروكالوميت و اكسيدهای فلزات بازی مانند اكسيد كلسيم، اكسيد روی يا اکسيد منيزيم [11].
غیر فعالکنندههای فلز (Metal deactivators)
یونهای فلزی مانند یونهای Ti ،Al و Cu، میتوانند تجزیه پلیمرها را تسریع کنند. این موضوع در جایی که پلیمرها در تماس مستقیم با فلز هستند، مانند سیمکشی و کابل، اهمیت ویژهای دارد. بهطور کلی، کاتالیزورهای فلزی مورد استفاده برای تشکیل پلیمر ممکن است بهسادگی در طول تولید در داخل آن محصور شوند. این معمولاً در مورد کاتالیزورهای زیگلر ناتا Ziegler Natta در پلیپروپیلن صادق است. در این موارد ممکن است غیر فعالکننده های فلزی برای بهبود پایداری اضافه شوند [11].
تثبیتکنندههای حرارتی
تثبیتکنندههای حرارتی بیشتر برای PVC استفاده میشوند، زیرا در معرض تخریب حرارتی هستند. این تثبیتکنندهها از دست دادن HCl را در فرآیند تخریب حرارتی که در دمای بالای 70 درجه سانتیگراد شروع میشود، به حداقل میرسانند [11] .
بازدارندههای شعله (Flame retardants)
بازدارندههای شعله طیف گستردهای از ترکیبات هستند که مقاومت پلیمرها در برابر آتش را بهبود میبخشند. بهعنوان مثال، میتوان به ترکیبات برم دار همراه با هیدروکسید آلومینیوم، تری اکسید آنتیموان و ارگانوفسفرههای مختلف اشاره کرد [11].
گردآورنده: ریحانه سفیری/ جمال الدین شاکری
منابع:
[1] https://en.wikipedia.org/wiki/Polymer_stabilizers
[2] https://doi.org/10.1002/pen.760100408
[3] https://doi.org/10.1016/C2011-0-07329-5
[4] https://blog.polymerdatabase.com/polymer%20chemistry/Antioxidants.html
[5] https://blog.polymerdatabase.com/polymer%20chemistry/Antiozonants.html
[6] https://doi.org/10.1016/C2011-0-07329-5
[7] https://blog.polymerdatabase.com/polymer%20chemistry/HALS.html
[8] https://doi.org/10.1016/C2011-0-07329-5
[9] https://www.otsukac.co.jp/en/products/ultraviolet-absorber
[10] https://www.gyc-speciality-chemicals.com/product/80/120
[11] https://doi.org/10.1016/C2011-0-07329-5